检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
光照与温度是调控植物生长发育的重要环境因子,由光敏色素B(phyB)作为受体感知。2022年钟上威实验室揭示了phyB通过光控蛋白质变构与温控液液相分离,实现对光照与温度两种不同环境信号的同时感知(Molecular Cell 82, 3015-3029)。自上个世纪50年代科学家发现光敏色素以来,围绕光敏色素的光激活、信号传导、生理功能等多方面取得了诸多进展,是国际植物生物学最受关注的研究领域之一。在光敏色素的信号转导中,有两个关键发现尤为瞩目。一个是Akira Nagatani实验室发现了phyB的细胞核定位现象:土壤中萌发的幼苗处于黑暗环境,phyB在细胞质中大量积累;出土见光后,phyB快速转入细胞核中行使功能。从细胞质向细胞核转运的入核称为phyB信号早期传导的关键限速步骤。另一个是Peter Quail实验室引领发现了phyB在细胞核内与转录因子PIFs直接互作,调控大量基因表达。自此,形成了广为熟知的phyB-PIFs模型,光信号通路的主流研究集中到了phyB在细胞核内的生理生化功能,但是,光诱导的phyB入核机制至今仍不清楚。
2023年3月16日,威尼斯wnsr666钟上威实验室在Cell期刊发表了题为“Sensory circuitry controls cytosolic calcium-mediated phytochrome B phototransduction”的研究论文,报道植物通过“光-钙调控环路”,快速激活两个钙依赖性蛋白激酶,在Ser80和Ser106位点磷酸化phyB,控制phyB入核。该工作同时提出了胞质第二信号钙离子在受体层面解码为特定转导通路的新机制。

在动物视觉感知中,钙离子作为第二信使参与了早期信号传导。上世纪80、90年代,科学家们通过生化抑制剂、微量注射等实验提示钙信号可能参与早期phyB的信号转导。但是由于抑制剂的非特异性影响、转导通路不清晰以及缺乏直接遗传证据,钙离子是否参与植物光信号通路存在很大争议。本研究中,作者利用稳定遗传的钙指示转基因植株,通过优化钙信号活体成像技术,避免叶绿素原酯、叶绿素等自发荧光的成像干扰,成功捕捉到在暗下生长的黄化苗见红光后,出现一个快速的胞质钙离子浓度上升信号,并通过红光-远红光可逆转换与遗传学证据,确定红光激发的胞质钙信号是由phyB所特异介导的(图1)。
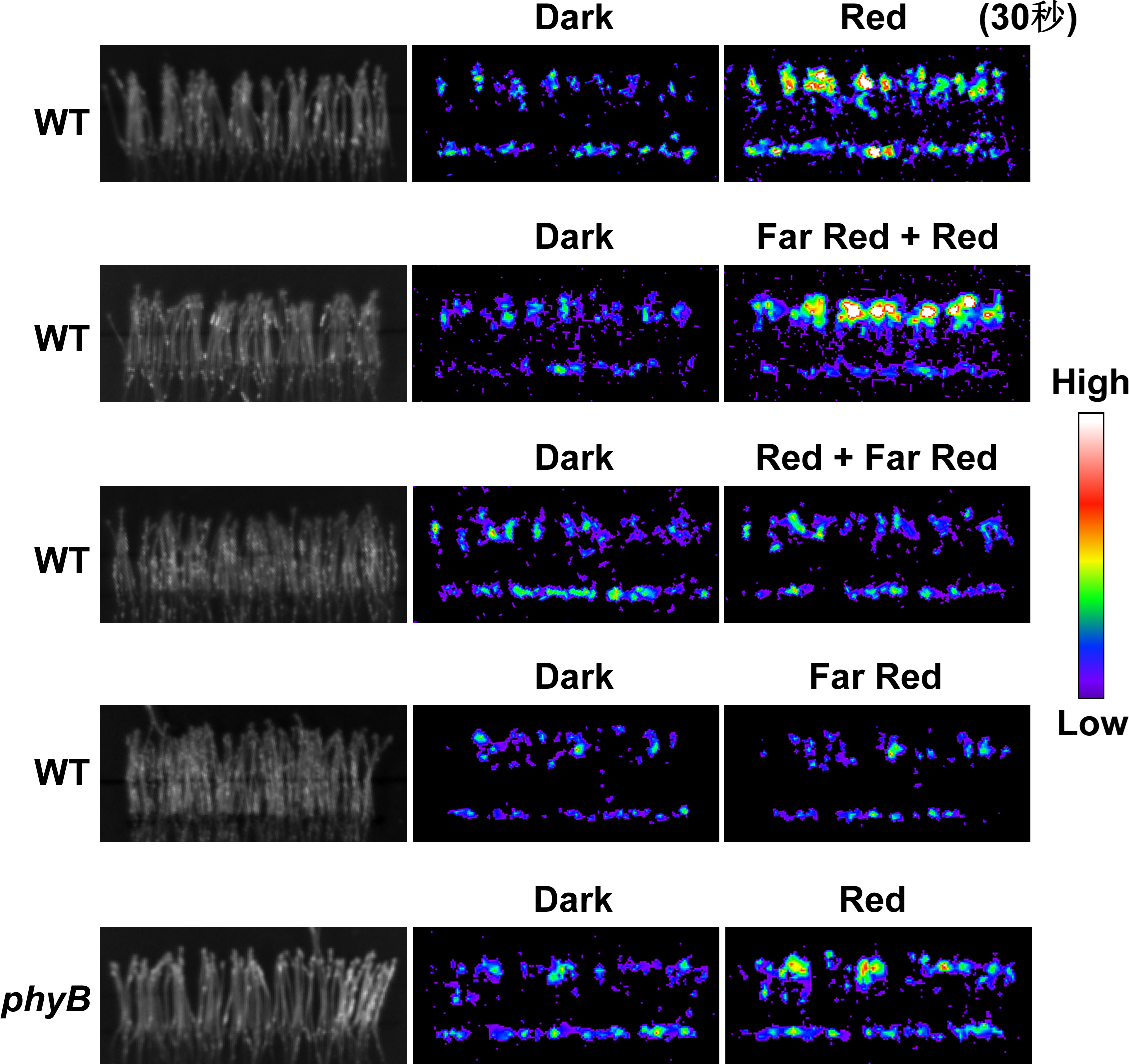
图1、红光通过phyB特异激活植物细胞质钙浓度升高。
暗下生长的黄化苗在处理前(Dark)与30秒红光处理后(Red),通过活体成像检测,发现红光能快速上调胞质钙浓度。当在红光处理后紧接着处理远红光,红光对胞质钙浓度的调控作用被逆转,暗示可能是由phyB介导(红光-远红光可逆调控是phyB的蛋白特性)。进一步通过遗传杂交,比较野生型(WT)和phyB突变体(phyB),发现phyB突变体中红光诱导的胞质钙浓度被显著降低,说明该过程主要由phyB所特异介导。
为了探究红光激活的胞质钙浓度升高是否具有生理功能,作者使用钙离子抑制剂对黄化苗进行了预处理,发现光响应基因的表达调控被显著抑制,说明钙离子可能参与了细胞核内的光信号响应。作者进一步检测了钙离子抑制剂对phyB入核的影响,发现当胞质钙离子信号被抑制后,光诱导的phyB入核被高度抑制,表明钙信号参与调控phyB入核。植物具有比动物更为丰富的钙结合蛋白解码系统。作者通过蛋白质互作筛选,鉴定到两个钙依赖性蛋白激酶CPK6和CPK12(CPK6/12)。当胞质钙浓度升高时,CPK6/12被激活,激活后的CPK6/12能特异识别红光激活的phyB,发生直接互作。当CPK6/12没有被钙激活,或者phyB没有被红光激活时,CPK6/12都不能识别phyB。只有在两者分别被钙和光同时激活的情况下,CPK6/12才能与phyB互作。CPK6/12识别phyB后,在phyB的Ser80和Ser106两个位点进行磷酸化修饰,使得phyB能够从细胞质转入细胞核,进而调控核内转录因子降解与光响应基因表达,促进植物幼苗子叶的快速打开与扩展,使其适应出土后的环境进行光合自养生长。
本论文中,作者提供了全面深入的分子遗传证据。在cpk6 cpk12双缺突变体中,红光诱导的phyB快速入核被显著抑制,且在黄化苗暗转红光12小时后,仍呈现子叶闭合与子叶不扩展的表型缺陷,与phyB突变体相似。当在cpk6 cpk12双缺突变体中转入组成型入核的phyB(phyB加上组成型核定位序列NLS,phyB-NLS),则能够完全恢复cpk6 cpk12双缺突变体的表型缺陷,表明该表型缺陷是由于phyB不能入核所导致。为了验证被CPK6、12磷酸化的Ser80和Ser106位点的生物学意义,作者构建了这两个位点磷酸化缺失的phyB-2A点突基因,与野生型phyB(phyB-WT)基因分别转入phyB突变体植物。亚细胞定位结果显示,黄化苗见光后,phyB-WT能快速入核,但phyB-2A不能入核(图2)。表型结果显示,phyB-2A幼苗在见光12小时后,子叶仍然保持闭合不扩展,呈现phyB突变体表型,而phyB-WT幼苗则正常发育。这些遗传证据与分子生化结果相互印证,表明CPK6/12通过磷酸化phyB的Ser80和Ser106位点调控phyB入核。
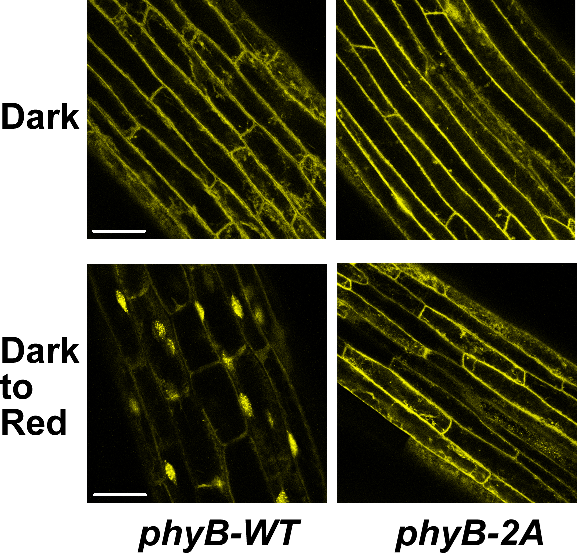
图2、Ser80和Ser106位点磷酸化是控制phyB入核的开关。
暗下生长的黄化苗在处理前(Dark)与2小时红光处理后(Dark to Red),观测phyB蛋白的亚细胞定位。结果显示,黄化苗细胞质中大量积累的phyB-WT,在见光2小时内即快速转入细胞核;当Ser80和Ser106位点被点突为磷酸化缺失的氨基酸后,phyB-2A蛋白不能入核。
此外,在种植转基因植物材料时,作者发现phyB-2A植物除了在黄化苗暗转光中出现发育缺陷,持续光照下,甚至在成年植株中都呈现phyB突变体表型,表明phyB-2A是一个没有生理功能的phyB点突蛋白。为了探究phyB-2A的功能缺陷是仅由于其不能入核,还是因蛋白活性受损导致,作者将phyB-2A加上NLS序列,使其定位于细胞核内。结果显示,phyB-2A-NLS恢复了所有phyB的功能,与phyB-WT没有区别,说明phyB-2A仅是影响了phyB入核,而蛋白的活性是正常的(图3)。作者进一步检测了cpk6 cpk12双缺突变体在其他光照条件下的表型,结果显示与phyB-2A的组成型入核缺陷不同,在cpk6 cpk12双缺突变体的黄化苗中,随着红光照射时间延长到24小时,phyB入核逐渐恢复。综合这些遗传结果,作者发现Ser80和Ser106位点磷酸化是控制phyB入核的广谱开关,而CPK6/12特异调控黄化苗见光引起的快速响应。植物可能通过不同的磷酸化途径来调控这两个位点,以适应复杂多变的环境。在黄化苗出土见光时,通过胞质钙浓度升高快速激活CPK6/12,介导胞质中大量积累的phyB在短时间内转入细胞核,促进环境剧变时的发育转变;而在长时间的稳定光照条件下,植物可能以其他激酶调控phyB的磷酸化与入核。

图3、Ser80和Ser106位点磷酸化特异控制phyB入核,但不影响phyB蛋白活性。
持续红光下生长的phyB-2A与phyB-9突变体表型相似,phyB-2A-NLS恢复正常生理功能,说明phyB-2A的功能缺失仅仅是由于其不能入核所导致。
综上所述,该研究发现红光通过phyB特异触发胞质钙浓度升高,激活钙依赖性蛋白激酶CPKs,被钙激活后,CPKs反过来与红光激活的phyB直接互作,磷酸化phyB使其入核,将红光激活的钙信号特异解码为核内光响应基因表达(图4)。先前研究发现,植物受到外界多种不同环境刺激时,比如盐碱、干旱、机械压力、低温以及虫咬等,都会诱发胞质钙浓度快速升高,激活钙依赖性蛋白激酶,但却最终产生与环境刺激相对应的特异生理响应。植物如何将通用的胞质钙信号解码成特异的生理响应一直是生物学关注的关键科学问题。该研究提出的“红光-phyB-Ca2+-CPKs-phyB”的“光-钙调控环路”中,CPKs-phyB元件需要光和钙信号的同时激活才能引起phyB入核,使得胞质钙浓度升高特异转换为光信号传导。在植物感知与响应环境变化中,环境信号受体是特异性最高的功能组分,该研究提出的“环境信号受体-钙信号-环境信号受体”调控环路机制,为深入认识钙信号的特异性解码提供新见解。
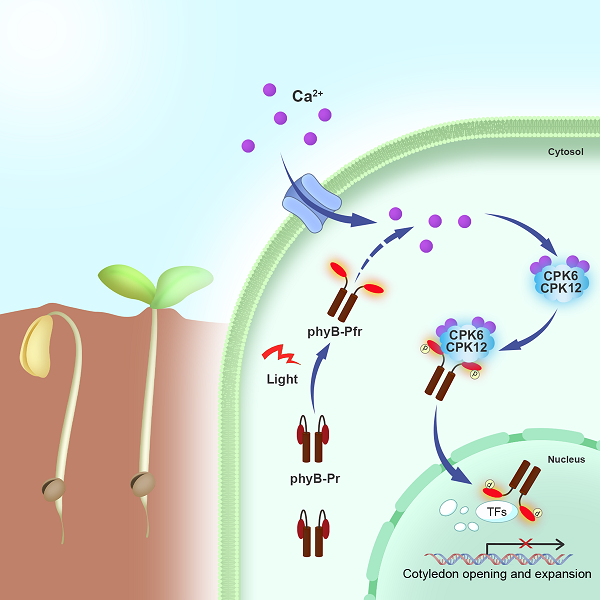
图4、出土幼苗通过“光-钙调控环路”,控制phyB入核。
出土前暗下生长的植物幼苗在细胞质中积累大量phyB,出土见光后phyB被红光激活,诱导胞质钙浓度快速升高,激活钙依赖性蛋白激酶CPK6/12,被钙激活的CPK6/12特异识别光激活的phyB,在Ser80和Ser106位点磷酸化phyB,使得phyB转变为能入核的形式,快速转入细胞核内,调控核内转录因子降解与光响应基因表达,促进出土幼苗形态发育转变。
威尼斯wnsr666、现代农业研究院钟上威研究员为该论文通讯作者,博士生赵晏、博士后施慧(现首都师范大学教授,PI)、已毕业博士潘颖为论文的并列第一作者,实验室成员吕默含、杨芷萱和寇小霞对论文做出了重要贡献。威尼斯wnsr666邓兴旺教授对该研究给予了大力支持。该研究得到了国家自然科学基金、蛋白质与植物基因研究国家重点实验室、启东-SLS创新基金和北京市属高校高水平教师队伍建设支持计划的资助。特别感谢威尼斯wnsr666凤凰工程仪器平台对本项目的技术支持。
钟上威实验室围绕光敏色素phyB的信号感知与传导发表了一系列工作,揭示了phyB“分子胶水”、“光解寡聚化”等调控新机制,为理解环境信号受体的功能模式提出了新的视角(Developmental Cell 39, 597-610;Developmental Cell 51, 78-88)。2022年,实验室揭示了phyB光小体的液液相分离形成机制,phyB通过光控蛋白质变构与温控液液相分离,实现对光照与温度两种不同环境信号的共感知机制(Molecular Cell 82, 3015-3029)。本研究历经8年的努力探索,提出的“光-钙调控环路”phyB入核调控机制,解决了领域内尚不清楚、存在争议的几个关键问题,审稿人称此项工作将“改变对光信号通路的现有认知”。
钟上威实验室致力研究植物幼苗出土存活的分子调控机制,诚聘不同学科背景的副研究员、助理研究员和博士后。实验室依托北大生命学院与现代农业研究院,将提供有竞争力的实验条件和个人待遇,欢迎联系。
原文链接:https://www.cell.com/cell/fulltext/S0092-8674(23)00128-9